Therapie von Glioblastomen
Motivation
Das Glioblastom, auch Glioblastoma multiforme (GBM) genannt, ist einer der häufigsten und aggressivsten menschlichen Hirntumore. Dieser Krebs lässt sich nur sehr schwer behandeln. Dies zeigt sich im Therapieerfolg, denn trotz multimodaler Herangehensweise, bestehend aus Operation, Chemo- und Strahlentherapie, liegt die mittlere Überlebenszeit von GBM-Patienten meist bei unter 15 Monaten. Auch die 5-Jahre-Überlebensrate der Patienten liegt sehr niedrig bei ca. 10 %. Ein entscheidendes Merkmal des GBM ist seine hohe Infiltrationsrate in das umgebende gesunde Gewebe, was zu einem hohen Wiederkehrrisiko (Rezidiv) des Tumors führt. Bei den meisten GBM-Patienten kommt es nur wenige Monate nach der Behandlung zu einem erneuten Auftreten des Tumors.
Ziele und Vorgehen
Unser Ziel ist es, die charakteristischen Eigenschaften, wie Invasivität und Migration, von Glioblastomazelllinien in Bezug auf therapeutische Behandlungen durch Bestrahlung und die Anwendung von Chemotherapeutika näher zu untersuchen, um dabei die Auswirkungen der Therapie auf die Beweglichkeit der Tumorzellen besser zu verstehen. Hierbei ist es wichtig, die zellulären Mechanismen zu identifizieren, die für die Entwicklung von Therapieresistenzen verantwortlich sind. In diesem Zusammenhang ist für uns die Rolle der zellulären Kommunikation zwischen den einzelnen Krebszellen als potenzieller Verursacher von Therapieresizenzen besonders interessant.
Innovationen und Perspektiven
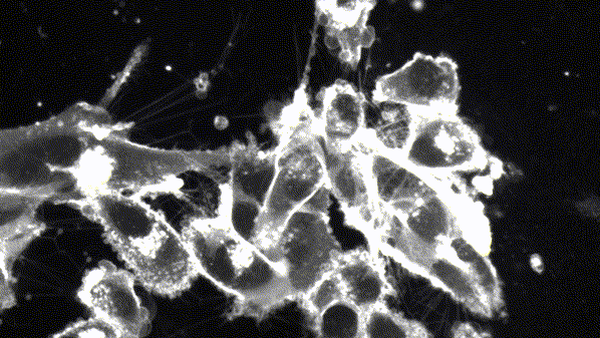
In unserer Forschung widmen wir uns den sogenannten Tunneling Nanotubes (TNTs), über die Zellen direkt miteinander kommunizieren können. TNTs sind Membranbrücken zwischen den einzelnen Zellen und ermöglichen somit einen schnellen und gezielten Austausch von Informationen. Besonders auffallend ist, dass die Krebszellen mithilfe der TNTs große, umfangreiche Kommunikationsnetzwerke ausbilden und sich somit optimal untereinander verständigen können. Diese Kommunikationsnetzwerke können möglicherweise dazu führen, dass die Krebszellen ihre Überlebensstrategien schnell anpassen und somit dem Abtöten durch die Therapie entkommen können.
Mithilfe unseres hochauflösenden Leica STED-Mikroskops sind wir in der Lage die Entwicklung der TNT-Netzwerke nach der Behandlung im Detail zu analysieren und deren Rolle in der Beweglichkeit der Krebszellen näher zu beleuchten.
Falls die TNT-Netzwerke zu dem aggressiven Verhalten von Glioblastomazellen beitragen, könnte man diese als Ziel für neue Therapieansätze verwenden und somit die Chancen auf eine erfolgreiche Behandlung von Glioblastomen erhöhen.